
Ethische Überlegungen zum Genome Editing am Menschen
Leitartikel von Alexander Massmann
Mit neuen Versuchen an Embryos möchten Forscher die Methoden des Genome Editing – oder der Genomchirurgie – perfektionieren, um Krankheiten zu lindern, zu heilen und ihnen vorzubeugen. Auch die vermeintliche genetische „Verbesserung“ gesunder Menschen wird diskutiert. Jüngst haben sich verschiedene Expertengremien zumindest im therapeutischen Bereich aufgeschlossen gezeigt. Dabei unterscheidet man somatische Eingriffe, also die Modifikation einzelner Zellen nach der Geburt, wobei Ei- und Samenzellen nicht betroffen sind, von Modifikationen der Keimbahn des Embryos. Auch wenn die somatischen Eingriffe von verschiedenen konkreten Faktoren eingeschränkt werden, dürften sie dennoch im menschlichen Anwendungsbereich am ehesten eine sinnvolle Perspektive bieten.
Im März diesen Jahres wurden zum ersten Mal Resultate der therapeutischen Genmodifikation an entwicklungsfähigen menschlichen Embryos veröffentlicht. Die beiden britischen und schwedischen Teams, die ebenfalls an menschlichen Embryos arbeiten, haben noch nicht veröffentlicht, und in früheren, aufsehenerregenden Studien aus China ging es um Embryos, die nicht entwicklungsfähig waren. Stets kam CRISPR-Cas9 zum Einsatz, das deutlich einfacher und günstiger ist als diejenigen Methoden der Genomchirurgie, die bereits seit ca. 15 Jahren entwickelt werden. Die jüngsten Resultate waren allerdings gemischt: Bei einem Embryo war technisch ein Erfolg zu verzeichnen, bei zweien wurde eine Mutation nur in manchen Zellen, nicht in allen korrigiert. In einem Embryo entstand eine neue Mutation, und bei zweien war keine Veränderung erkennbar.
Was bedeutet der gegenwärtige Stand der Forschung?
Aus technischer Sicht sind die Resultate weder ein Triumph noch ein Rückschlag, doch besonders die Entstehung einer neuen Mutation ist signifikant. Bei diesem Stand der Technik hält niemand eine Implantation eines genmodifizierten Embryos für verantwortbar. Zugleich sehen Experten großes Entwicklungspotential in den Methoden des Genome Editing, und die chinesischen Experimente sind für sie eine Station auf dem Wege, das „Skalpell“ der Genomchirurgie zu schärfen und zu perfektionieren. Bei diesem Ziel geht es nicht bloß um eine begrenzte Zahl sogenannter somatischer Zellen (Körperzellen). Aus den embryonalen Zellen entwickeln sich sämtliche Zellen des menschlichen Körpers, und genetische Veränderungen hier finden sich nicht nur in den Körperzellen des reifen Organismus, sondern auch in den Geschlechtszellen, so dass Modifikationen an Nachkommen vererbt würden. Das ist der entscheidende Punkt, wenn man die Embryonalzellen als die Keimbahn bezeichnet.
Zeitgleich zu diesen Versuchen trat im Frühjahr auch die juristische und ethische Diskussion in ein neues Stadium ein. Die amerikanischen Akademien der Wissenschaften sprachen sich dafür aus, die therapeutische Genmodifikation von Embryos zuzulassen, sofern man die technischen Risiken im Griff hat. Da die USA international das Schwergewicht der molekularbiologischen Forschung sind, hätte eine neue Weichenstellung dort bedeutende Folgen. Der Rat der Europäischen Akademien der Wissenschaften (EASAC) veröffentlichte daraufhin eine Empfehlung, die gegenüber Keimbahneingriffen aufgeschlossen ist. In Deutschland hatte sich vor zwei Jahren die Nationale Akademie der Wissenschaften, die Leopoldina, gemeinsam mit der DFG abwägend zum Thema geäußert, wie auch die Berlin-Brandenburgische Akademie der Wissenschaften. Der Deutsche Ethikrat befasste sich auf der Jahrestagung 2016 mit dem Thema und veranstaltete zudem ein Treffen mit britischen und französischen Experten. Im März 2017 gab die Leopoldina nun ein „Diskussionspapier“ von elf Autorinnen und Autoren heraus, die eine Änderung des deutschen Embryonenschutzgesetzes empfehlen: Es solle die Forschung an solchen Embryos ermöglicht werden, die im Zuge der künstlichen Befruchtung entstanden sind, sich aber aufgrund einer irregulären Chromosomenausstattung prinzipiell nicht implantieren lassen. Aus der Forschung an Embryos dürfte sich ein besseres Verständnis der menschlichen Embryonalentwicklung ergeben, was auch der Fortpflanzungstechnologie zugutekommen kann. Außerdem verspreche die Forschung an Embryos Fortschritte bei somatischen Gentherapien, aber auch bei Keimbahntherapien.
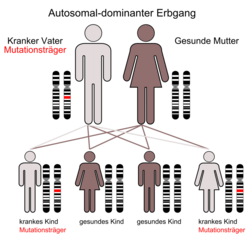
Traditionell steht hinter solchen Vorschlägen die Hoffnung, dass Eltern mit belastenden genetischen Mutationen Kinder bekommen können, die nicht selbst von schweren Krankheiten direkt betroffen sind. Das klassische Beispiel ist die Chorea Huntington: Trägern der entsprechenden genetischen Mutation steht zunehmende und schließlich schwere Demenz bevor, und auch die elementare körperliche Koordination nimmt schrittweise ab. Symptome der unheilbaren Krankheit setzen etwa zwischen dem 30. und 50. Lebensjahr ein. Betroffene geben mit einer Wahrscheinlichkeit von 50% das Gen an Nachkommen weiter, und bei Vererbung durch einen Elternteil ist der Beginn der Symptome eine Frage der Zeit. Ist der Embryo mehrere Wochen alt, kann auch die Genomchirurgie keine Abhilfe verschaffen; die betroffenen Zellen des entwickelten Organismus sind zu zahlreich und unzugänglich. Ein potentieller therapeutischer Eingriff in die Keimbahn des frühen Embryos würde nicht mehr und nicht weniger als Prävention bedeuten. Vergleichbare Krankheiten, wenn auch mit deutlich anderen Symptomen, sind etwa Muskeldystrophien und die Mukoviszidose.
Doch Kritiker nehmen nicht nur Anstoß daran, dass die Forschung an Embryos menschliche Lebewesen verwendet. Darüber hinaus könnte es scheinen, dass bei der therapeutischen Modifikation von Genen die Substanz des Menschlichen zur Disposition gestellt werde – und bekanntlich erregen bereits genmodifizierte Pflanzen die Gemüter. Inwieweit sind ferner die Folgen tatsächlich absehbar, auch über Generationen hinweg? Und bleibt es beim therapeutischen Ansatz? In angesehenen Fachzeitschriften erscheinen verschiedentlich Berichte über menschliche Gen-Varianten, die angeblich zur Intelligenz beitragen (wobei dahingestellt sei, wie man Intelligenz definiert). Die amerikanischen Wissenschaftsakademien befürworten zwar therapeutische Keimbahneingriffe, wollten aber „zu diesem Zeitpunkt“ keine Empfehlung zugunsten weitergehender, vermeintlich ‚verbessernder‘ Veränderungen abgeben. Der Bericht der New York Times über diese Stellungnahme gab einem Forscher das Wort, der fragte, weshalb man eigentlich nicht die Stellschrauben noch ein wenig weiterdrehen sollte, wenn man sich ohnehin schon an das Genom des Embryos wagt. Der Rat der Europäischen Akademien der Wissenschaften zeigt sich hier ebenfalls aufgeschlossen. Das Diskussionspapier aus dem Kreise der Leopoldina lehnt eine „genetische Verbesserung“ von Embryos ab mit dem Hinweis auf naturwissenschaftliche Unklarheiten, aber auch aufgrund des gesellschaftlichen Diskussionsbedarfs. Wenn der Nuffield Council on Bioethics, ein in Großbritannien sehr angesehener Ethikrat, seine Stellungnahme zum Genome Editing demnächst abschließt, dürfte die entscheidende Frage dort lauten, ob die Tür zu „Enhancements“ offengehalten wird.
Die öffentliche Diskussion nachjustieren
Der Debatte um therapeutische Eingriffe in die Keimbahn sollte man sich nicht prinzipiell verschließen mit dem pauschalen Hinweis, dass die zukünftigen Folgen von Keimbahninterventionen unabsehbar und deshalb unvertretbar sind. So lautet die Argumentation mit dem Vorsichtsprinzip, das verschiedentlich etwa in kirchlichen Kreisen angeführt wird. Doch es sind auch die Folgen unterlassener Handlungen zu bedenken, so dass potentiell auch der Verzicht auf hilfreiche Maßnahmen zu Buche schlägt. Auf den potentiellen Nutzen von Keimbahninterventionen ist freilich noch zurückzukommen.
Eine weitere Frage lautet, wie die Debatte um Keimbahneingriffe unser Verständnis des menschlichen Lebens verändern kann. Gewiss ist ein Mensch wesentlich mehr als sein Genom. Es wäre aber zu bedauern, wenn eine Debatte über Modifikationen des menschlichen Erbgutes unter dem Eindruck unrealistisch großer Möglichkeiten geführt würde und die Vorstellung der künstlichen Plastizität des Menschen normalisiert würde. Mehrere Grenzen des Genome Editing sollten deshalb stets kommuniziert werden. Verfechter sollten z.B. nicht pauschal auf Krankheiten verweisen, die sich mit dem Genome Editing angehen ließen. Gewiss wird das Genome Editing oft als transformativ, geradezu bahnbrechend bezeichnet. Ein Grund liegt darin, dass es die Verhinderung vieler gravierender Krankheiten ‒ möglicherweise aller bekannten monogenetischen Krankheiten ‒ verspricht. Die Vorstellung, die Eigenschaften eines Menschen im Prinzip modellieren zu können, ohne dabei von den bestehenden Eigenschaften von Zellen eingeschränkt zu werden, die zudem möglicherweise schwer zugänglich sind, hat gewiss große Faszinationskraft. Die Hoffnungen auf genetische „Verbesserungen“ trägt für manche zudem zur Attraktivität der Keimbahnintervention bei. Allerdings hat es die Keimbahnintervention gerade nicht mit der Heilung von bestehenden, symptomatischen Krankheiten oder der Behebung von genetischen Dispositionen nach der Geburt zu tun. Dagegen fragt sich, ob der eigentliche Nutzen des Genome Editing nicht eher in Modifikationen am geborenen Menschen besteht, wenn es überhaupt um das menschliche Genom gehen soll. Solche Modifikationen sind allerdings nur in sehr bestimmten Fällen wirksam.
Zudem wird oft stillschweigend vorausgesetzt, dass sich Interessenten mit belastenden Erbanlagen für die künstliche Befruchtung (IVF) entscheiden würden. Wenn sie das möchten und auch können, ist es ihnen in der Zukunft potentiell möglich, dass sie in der Familienplanung von neuen medizinischen Methoden profitieren. In dieser Situation ist die Keimbahnmodifikation allerdings nicht ohne Alternativen. Andererseits könnten Betroffene auch die natürliche Empfängnis vorziehen und somit auf die Genchirurgie verzichten. Sollte der Nachwuchs ebenfalls von genetisch bedingten Erkrankungen betroffen sein, könnten die Eltern möglicherweise auf herkömmliche Behandlungsmethoden setzen, mit ihren Möglichkeiten und Grenzen. Leicht diffuse Aussichten, bestimmte Erkrankungen mit Keimbahninterventionen angehen zu können, sprechen jedoch nicht pauschal für dieses Verfahren.
Zumindest im englischsprachigen Diskurs lässt sich ferner eine eigenartige Erscheinung beobachten. Manche Autoren erzeugen einerseits große Aufmerksamkeit für Genmodifikationen am Menschen mit dem Argument, dass sich hier epochale Möglichkeiten auftun. Sobald Skeptiker andererseits einwenden, dass solche Eingriffe zu weit gehen könnten, lautet die Verteidigung, dass diese Kritiker lediglich einem verstaubten Gendeterminismus anhängen – also der Ansicht, dass genetische Variationen zwangsläufig zu deutlich messbaren Veränderungen am Organismus führen. Die Kritik am Gendeterminismus könnte jedoch auch die Resonanz genetischer Eingriffe relativieren. Tatsächlich ist unbestritten, dass – abgesehen von bestimmten monogenetischen Erbkrankheiten – Umweltfaktoren und Verhalten eine bedeutende Rolle spielen für die Eigenschaften des Organismus. Ob modifiziert oder nicht, die Gene sind nicht gleichbedeutend mit dem Schicksal. Man sollte aber die Faszination für genetische Eingriffe nicht unnötig befeuern, auch nicht mit der alten, nach wie vor anzutreffenden eugenischen Redeweise, dass wir die Zügel der Evolution nun endlich selbst in die Hand nehmen könnten. Selbst schräge Projekte wie die Wiederbelebung von Wollmammuts oder Neandertalern durch Genmodifikation erzielen beachtliche Effekte auch in deutschen Medien. Ein Bericht über genmodifizierten Reis mit hohem Vitamin-A-Gehalt kann sehr guter Journalismus sein; das gilt aber nicht von der Ansicht, dass das Genome Editing das Welthungerproblem lösen dürfte oder auch zum Albtraum einer genetisch herangezüchteten Kriegerkaste führen könnte (so kürzlich das Magazin „Wired“).
Wenn das wissenschaftliche Interesse der Bürgerinnen und Bürger geweckt wird, ist das zu begrüßen. Eine mögliche negative Folge allzu plakativer Ansichten über die Auswirkungen der Genmodifikation am Menschen könnte etwa darin bestehen, dass die Furcht, der eigene Nachwuchs könnte vom Ideal abweichen, unverhältnismäßig wächst. Könnte die gesellschaftliche Solidarität mit Menschen mit Behinderung abnehmen, wenn Behinderungen zunehmend vermeidbar würden? Hier wenden Verfechter neuer technischer Möglichkeiten ein, dass die Entstehung von subtilem gesellschaftlichem Druck zwar nicht wünschenswert ist; solcher Druck sollte uns aber nicht davon abhalten, die reproduktive Autonomie von Bürgerinnen und Bürgern zu stärken, wo es realistisch ist. Ein konstruktiver Vorschlag kann hier lauten, dass medizinisch sinnvolle genetische Eingriffe von erneuten öffentlichen Investitionen begleitet werden sollten, die Menschen mit Behinderung den Alltag erleichtern, etwa ihre Inklusion im Schulunterricht realistischer machen. Der Gewinn an reproduktiver Autonomie sollte nicht allein darin bestehen, dass sich Behinderungen zunehmend verhindern lassen, sondern auch darin, dass ein Leben mit Behinderung erleichtert wird.
Worin liegt der Mehrwert einer Keimbahnmodifikation?
Die Frage des Gendeterminismus ist noch in anderer Hinsicht relevant. Abgesehen von den genannten monogenetischen Krankheiten bestimmen normalerweise auch Umwelteinflüsse und individueller Lebensstil die Eigenschaften des Organismus mit. Das heißt einerseits, dass ein Molekularbiologe, der genetische Eingriffe vornimmt, nicht „Gott spielt“. Andererseits sollte der Wunsch zur Verhinderung bestimmter Krankheiten nicht in jedem Falle genetische Modifikationen legitimieren. Beispielsweise ist die Schizophrenie unter anderem auch genetisch bedingt – um ein Beispiel zu wählen, das auch in der deutschen Fachdebatte bemüht wird. Vieles an dieser Krankheit ist medizinisch rätselhaft. Fest steht immerhin, dass sich aus einer genetischen Veranlagung zur Schizophrenie noch längst kein signifikantes Risiko von Symptomen ableiten lässt. Ebenfalls lässt sich aus dem Auftreten von Schizophrenie-Symptomen bei einem Erwachsenen nicht unbedingt ein Schizophrenie-Risiko für den Nachwuchs folgern. Oft kann ein verantwortlicher Lebensstil das Schizophrenie-Risiko weitgehend minimieren. Deshalb sollte gerade die Schizophrenie nicht als Beispiel dafür herangezogen werden, dass genetische Keimbahneingriffe oft das Mittel der Wahl wären.
Es kommt hinzu, dass bei bestimmten Krankheiten die Präimplantations-Diagnostik (PID) bereits Möglichkeiten bietet, eine besondere genetische Belastung des Nachwuchses zu verhindern. Wenn ein Elternteil eine Prädisposition zu einer signifikanten genetischen Erkrankung in sich trägt, kann das Paar die künstliche Befruchtung wählen und daraufhin die resultierenden Embryos genetisch untersuchen lassen. Die Implantation eines bestimmten Embryos kann das Paar dann davon abhängig machen, ob er von dem entsprechenden Risikofaktor frei ist. Die PID ist technisch wesentlich weniger riskant als das Genome Editing und eignet sich bei Krankheiten wie der Chorea Huntington, deren genetische Disposition sich auf ein einzelnes Gen eingrenzen lässt. Da Keimbahninterventionen ohnehin der Prävention dienen und die künstliche Befruchtung erfordern, ist die PID in der Regel eine sinnvolle Alternative. Besonders wenn sie von öffentlichen Investitionen begleitet wird, die das Leben mit Behinderung erleichtern, sollte sie nicht als negative Eugenik verunglimpft werden. In der Tat kann für ihre größere soziale Akzeptanz sprechen, dass hier weniger Anlass besteht, Tendenzen zur Eugenik zu befürchten. Denn wo das Gene Editing prinzipiell die Schaffung neuer Erbanlagen erlaubt und Fragen zur „Verbesserung“ der Nachkommen aufwirft, hat es die PID nur mit dem Vergleich zwischen dem Genom bestehender Embryos zu tun.
Die PID wäre allerdings wenig geeignet, wenn ein Elternteil mehrere problematische Gene hat, von denen auch nur eine Teilmenge das Krankheitsrisiko klar erhöht. Bei einer solchen polygenetischen Prädisposition sinkt die Wahrscheinlichkeit, dass eine ausreichende Zahl „gesunder“ Embryos gewonnen werden kann und es letztlich zur Schwangerschaft kommt. Denn es können der Frau zwecks IVF nur eine begrenzte Zahl an Eizellen entnommen werden. Die Zahl geeigneter Embryos wird per PID dann verringert, und bei der künstlichen Befruchtung kommt es - ähnlich wie bei der natürlichen Zeugung - nur bei einem Teil der Embryos zu einer erfolgreichen Einnistung. Polygenetische Prädisposition liegt etwa bei der Schizophrenie vor, was gegen die PID sprechen könnte. Doch hier gilt wieder, dass genetische Risikofaktoren für sich genommen nicht notwendigerweise medizinisch signifikant sind. Andere Faktoren könnten eine Erkrankung nur in einem sehr moderaten Maße wahrscheinlich machen, so dass die Risken der Genomchirurgie vielleicht nicht geringer sind als die der bestehenden genetischen Veranlagung.
Andererseits könnten polygenetische Prädispositionen zum Krebs führen. Bei bei den öffentlichkeitswirksamen Beispielen bestimmter BRCA-Mutationen ist das allerdings nicht oder nur eingeschränkt der Fall. Zu Krebs-Risikofaktoren, die tatsächlich polygenetisch agieren und bei denen PID nicht geeignet wäre, argumentiert allerdings John Parrington („Redesigning Life“), dass zahlreiche genetische Prädispositionen sehr individuelle Formen annehmen können. Woher wissen wir, welche Änderungen tatsächlich „herauseditiert“ werden müssten, um das Krebsrisiko signifikant zu senken? Hier ist also die Genmodifikation weniger interessant als bestehende Möglichkeiten der Prävention und Therapie.
Ein weiterer Einwand gegen die Bedeutung der PID besagt, dass beide Elternteile zugleich eine Veranlagung zu einer monogenetischen Erkrankung tragen können. Die Erfolgsaussichten einer typischen PID wären hier deutlich vermindert: Statistisch ist nur ein Viertel der gewonnenen Embryos frei von den kritischen Anlagen, womit die Chancen einer erfolgreichen Implantation deutlich sinken. Vertreter dieses Arguments räumen ein, dass diese Konstellation sehr selten sein dürfte. Denkbar ist es allerdings auch, Ei- und Samenzellen vor der Befruchtung gesondert genetisch zu untersuchen und auszuwählen.
Die Bedeutung dieser Diskussion liegt einerseits darin, dass die PID in verschiedenen Fällen eine Alternative zu Keimbahninterventionen bietet. Sie wird in einschlägigen Verlautbarungen jedoch selten hinreichend gewürdigt. Andererseits sind biomedizinische Eingriffe keineswegs bei allen Krankheitsbildern angezeigt. In vielen Fällen steht die Antwort noch aus, worin genau der Mehrwert einer Keimbahnmodifikation liegt.

Somatische Genmodifikationen
Im Augenblick befindet sich die öffentliche Aufmerksamkeit für das Genome Editing in einer Schieflage. Denn einerseits lenken die Möglichkeiten der Keimbahnintervention große Aufmerksamkeit auf sich, deren Nutzen aber noch nicht deutlich ist. Die Faszinationskraft sehr weitreichender biotechnologischer Eingriffe, laut manchen Autoren gar des Wandels der menschlichen Spezies, tut außerdem ihren Teil. Demgegenüber sind somatische Anwendungen des Genome Editing, bei denen Ei- und Samenzellen nicht betroffen sind, nachdrücklich zu würdigen. Sie werden manchmal pauschal zur Legitimation des Genome Editing angeführt, obwohl sie von Keimbahneingriffen klar zu unterscheiden sind. Somatische Eingriffe können Risiken auch dadurch vermindern, dass man dem Körper Zellen entnimmt, sie verändert, prüft und wieder einsetzt. Da die somatische Modifikation stromabwärts statt stromaufwärts ansetzt, also nicht bei den wenigen Zellen am Anfang der Entwicklung, ist die Anzahl der betroffenen Zellen geringer, was das Risiko vermindert. Hier bedeuten zudem ältere Verfahren des Genome Editing einen geringeren Bedarf der Forschung an Embryos.
Zuzugestehen ist sicherlich, dass somatische Genmodifikationen von bedeutenden Restriktionen beeinträchtigt sind. So scheitern sie verschiedentlich daran, dass verschiedene Arten von körperlichem Gewebe schlecht oder gar nicht zugänglich sind – insbesondere Hirnzellen, die gerade von gravierenden neurodegenerativen Krankheiten betroffen sein können. Doch manche Krankheiten lassen sich mit somatischen Genmodifikationen anscheinend bereits therapieren. So kann die genetische Modifikation weißer Blutkörperchen bestehende Blutkrebs-Therapien entscheidend unterstützen. Ein Londoner Kinderkrankenhaus hat so anscheinend bereits mehrere Leben gerettet. Bei einem Krankheitsbild namens SCID (schwerer kombinierter Immundefekt) bedeutet die genetische Modifikation von Körperzellen ebenfalls einen wesentlichen Durchbruch. Vielversprechende Ansätze zur Heilung von HIV/AIDS im somatischen Bereich bestehen ebenfalls, was immerhin einen Fortschritt zur gegenwärtigen medikamentösen Stabilisierung bedeutet.
In verschiedenen Fällen dürfte die somatische Genmodifikation Symptome immerhin erleichtern. Bei Mäusen, die Muskeldystrophien aufweisen, konnten deutliche Verbesserungen erzielt werden, auch wenn eine Heilung unrealistisch scheint. Da die Blutbahn für genetische Modifikationen gut erreichbar ist und größere Mengen Blut die Leber passieren, lässt sich auch ein gewisser Anteil von Leberzellen genetisch modifizieren. In Mäusen wurden Krankheitssymptome im Harnstoffzyklus gemildert, und eine amerikanische Firma führt klinische Studien durch, von denen man sich gar eine Heilung der Hämophilie (Bluterkrankheit) erhofft. Diese Firma arbeitet ebenfalls an Möglichkeiten, in bestimmten Fällen die Symptome von Morbus Hunter zu mildern. Neben Blutbahn und Niere ist auch das Auge prinzipiell für therapeutische Genmodifikationen geeignet. Ob auch Zellen für die Genomchirurgie erreichbar sind, die bestimmte Formen des Diabetes verursachen, ist Gegenstand der Forschung.
Genetische „Verbesserung“?
Damit ist noch die Frage nach genetischen „Verbesserungen“ ("Enhancements") offen. Während zahlreiche Statements pauschal auf offensichtliche wissenschaftliche Unsicherheiten und Vorbehalte in der öffentlichen Meinung verweisen, argumentiert der Rat der Europäischen Akademien der Wissenschaften, dass Enhancements legitim sein können, solange sie keine sozialen Ungleichgewichte schaffen und kein Zwang herrscht. Hier geht es gewiss um Vermeidung eugenischer Praktiken. Es muss allerdings Klarheit bestehen, dass solche Enhancements im wesentlichen Keimbahneingriffe wären. Mit somatischen Eingriffen lassen sich meistens nicht hinreichend große Effekte erzielen. Keimbahneingriffe setzen jedoch am Embryo an, so dass die eigentlich Betroffenen nicht einwilligen können. Gewiss treffen Eltern stets Entscheidungen für ihre Kinder. Doch gerade damit ist die Aufgabe gestellt, mit Kindern nicht auf manipulative oder autoritäre Art umzugehen. Zu Recht setzt sich die Pädagogik in Schulen und Gemeinden etwa für eine Erziehung zur Autonomie ein, so dass kindgemäße Unterrichtsmethoden an die Stelle des Mottos „Friss, Vogel, oder stirb“ treten. Andererseits neigen Eltern mit zu großem Ehrgeiz oder allzu starkem Behütungsinstinkt („Helikopter-Eltern“) auch ohne Genmodifikationen dazu, Kinder in ihrem Bilde zu formen.
Ein bekanntes Foto eines „Bambinilaufs“ aus dem vergangenen Jahr zeigt, wie ambitionierte Eltern ihre unwilligen Kinder über die Ziellinie zerren. Man stelle sich vor, Eltern unterziehen sich der aufwendigen künstlichen Befruchtung und nehmen große Kosten für genetische „Verbesserungen“ in Kauf, die zudem nie ganz ohne medizinisches Risiko denkbar sind. Dass solche Eltern ihre Kinder nicht zusätzlich unter Druck setzen würden, dürfte unrealistisch sein. Genmodifikationen am Menschen sind in bestimmten Fällen positiv zu würdigen, doch Enhancements zählen nicht dazu. Die Grenzen somatischer Eingriffe verweisen uns außerdem wieder auf die alte Frage, wie wir mit Unvollkommenheiten und Grenzen umgehen – können wir sie nicht in vielen Fällen auch als typisch menschlich würdigen?
Alexander Massmann
Veröffentlicht im Juli 2017
Sie lesen lieber aus einem Buch? Sie finden diesen Artikel auch in unserem zweiten Buch zu dieser Webseite, "Die Vermessung der Welt und die Frage nach Gott" (Bonn 2018). 18 Beiträge von renommierten Autoren, darunter auch ein Nobelpreisträger, führen in den Dialog mit der Wissenschaft angesichts der Gottesfrage ein.
Bildnachweis
Doctor touched medical clamp a DNA. #159700481 @fotolia.com | Urheber: natali_mis
Autosomal-rezessiver Erbgang @wikimedia commons | Urheber: Armin Kübelbeck
DNA Encoding and Genetic Code #104562633 @fotolia.com | Urheber: kentoh
CRISPR/Cas9 system for editing, regulating and targeting genomes #101640233 @fotolia.com | Urheber: ibreakstock
Sportmediapics.com/Manfred Binder
Diesen Beitrag fand ich...
Genomediting am Menschen
Was erwarten, erhoffen und befürchten Sie von den neuen Möglichkeiten?
Alexander Massmann diskutiert Möglichkeiten und Risiken von somatischen Operationen ebenso wie Eingriffen in die Keimbahn des Menschen. Was denken Sie darüber?




Kommentare (0) Keine Kommentare gefunden!